幼年特发性关节炎,不只有骨关节症状
幼年特发性关节炎(JIA)是一种儿童时期常见的慢性疾病,定义为:16岁以下儿童不明原因关节肿、痛、热或活动受限,持续6周以上。JIA包括7个亚型,即:全身型(sJIA)、少关节炎型(持续型或扩展型,oJIA)、类风湿因子阳性多关节炎型 [(RF+)pJIA]、RF阴性多关节炎型 [(RF-)pJIA] 、附着点炎相关性关节炎型(ERA)、银屑病性关节炎型(PsA)以及未分化性关节炎,第7型定义为不符合上述任何1项或符合上述2项以上标准的关节炎。
JIA病程长,很多患儿(31%-55%)进入成年期后病情仍处于活动期[1]。疾病表现复杂多样,易迁延复发,给疾病的诊疗带来了极大的困难。该疾病关节畸形发生率较高,是小儿残疾的主要原因之一。多关节型幼年特发性关节炎(pJIA)定义为在起病后6个月内受累的关节超过≥5个,为JIA中治疗较为棘手的一种亚型,如果诊断治疗不规范,pJIA患儿的关节畸形发生率高达46.1%[2],值得高度关注。

JIA病因与发病机制尚不明确,目前普遍认为是一组与遗传特质、免疫紊乱、环境因素高度关联的异质性疾病。值得注意的是,虽然JIA以慢性关节滑膜炎为主要特征,但并非单纯的骨关节表现,疾病可累及全身,患者往往伴有不同程度机体各器官、组织损害。其常见的合并症/并发症包括生长迟缓、葡萄膜炎、巨噬细胞活化综合征(MAS)、心肌酶升高、心律失常及心包积液等心脏并发症、反复胸膜炎、间质性肺病变、中枢神经系统并发症等。
不同亚型JIA的常见合并症有所区别,对后续的治疗选择具有一定参考价值。如全身型JIA的常见并发症有贫血、心包炎、MAS等,而pJIA患者则常见眼部并发症如葡萄膜炎。
当前,JIA治疗的主要目标包括控制病变的活动度,减轻或消除关节疼痛和肿胀,预防感染和关节炎症加重,预防关节功能不全和残废,恢复关节功能及劳动能力。在治疗患儿骨关节症状的同时,不能忽视其他系统性合并症及治疗过程中可能出现的全身不良反应。
减少激素不良反应,
阿达木单抗强效维持患儿正常生长
约10%-40%JIA患者会出现身材矮小,生长迟缓在全身型JIA和pJIA患儿中更为严重[3]。这可能是由于患儿高水平的促炎细胞因子导致生长激素分泌减少、抑制长骨生长。此外,医生普遍认为,激素的应用也是引起患儿生长迟缓、青春期延迟的重要原因。激素治疗引发的骨密度降低、骨折等风险同样值得高度警惕。

糖皮质激素可用于JIA治疗,但主要推荐用于全身型JIA,而多关节型、少关节型、银屑病相关型和附着点相关型,一般不建议全身使用糖皮质激素。对这些类型的JIA患者,仅当关节症状明显、累及主要脏器功能、出现葡萄膜炎等并发症或实验室指标明显异常时推荐加用糖皮质激素治疗[4]。
近年,随着对自身免疫性疾病的深入探索,人们已经逐渐认识到,细胞因子在这类疾病中发挥了关键性的作用。其中,TNF-α参与了JIA等多种免疫介导性疾病,是发病机制中的核心因子[5]。靶向抑制TNF-α的生物治疗能快速起效并持续改善JIA患儿骨关节症状,还可通过缓解全身炎症,帮助患者得到更全面的获益,在JIA传统治疗与管理模式基础上,成为JIA治疗领域又一项里程碑式的进展。2019年,全球首个全人源抗TNF-α单抗——原研阿达木单抗在国内获批用于pJIA治疗,成为中国大陆首个且唯一获批用于pJIA的生物制剂,给广大pJIA患儿带来了新的选择。
研究表明,阿达木单抗可强效维持pJIA幼龄患者(2-4岁)的正常生长,为患儿带来全面、长期的获益(图1)[6]。
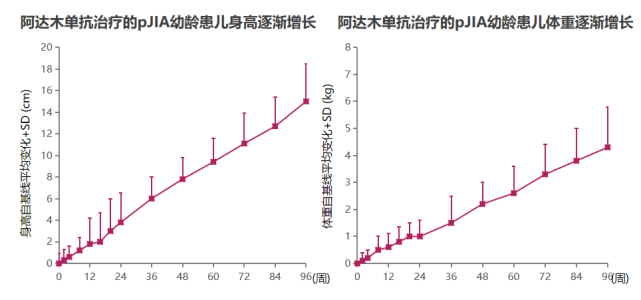
图1 阿达木单抗维持pJIA幼龄患儿的正常生长
一项事后分析描述了经阿达木单抗治疗的pJIA患儿的生长参数。研究纳入了DE038研究中的171例4-17岁pJIA患儿,按基线权重分为2组:≤33rd百分位组或小于33rd百分位组,结果表明,pJIA患儿接受阿达木单抗治疗104周,身高自基线逐渐增长,证实阿达木单抗可改善并维持pJIA患儿的正常生长(图2)[7]。

图2 阿达木单抗改善并维持pJIA患儿的正常生长
备注:≤33rd百分位&>33rd百分位:依据美国疾病控制和预防中心(CDC)身高增长图表
关注JIA患儿眼部健康,积极治疗葡萄膜炎
葡萄膜炎为JIA最常见的一种关节外表现[8]。据统计,JIA的患者中约11%-30%的患者合并葡萄膜炎。由于缺乏明显的眼部症状,如发红、疼痛或光敏感,诊断可能会被忽略。如不及时治疗会出现并发症,严重威胁视力,如带状角膜病变、白内障、青光眼或低眼压等[9]。
糖皮质激素是治疗葡萄膜炎的常用药,但应避免长期使用,以避免严重不良反应。糖皮质激素的主要不良反应为眼压升高。长期外用糖皮质激素或局部糖皮质激素注射可导致眼不良反应,如白内障和青光眼,长期使用全身糖皮质激素可导致严重的不良反应,如生长发育迟缓、肾上腺抑制、骨骺过早闭合、高血糖、感染和骨质疏松等[9]。因此,治疗时应早期联合传统DMARDs和/或生物制剂,以尽快缓解疾病,迅速减停激素,减少不良反应。
SYCAMORE研究为一项多中心、随机、双盲、安慰剂对照研究,旨在评估阿达木单抗对JIA相关性葡萄膜炎的疗效,共纳入90例2岁以上的JIA患儿,其中pJIA 14例,oJIA 74例,PsA 2例。随机分为阿达木单抗组 (n=60)和安慰剂组(n=30)。主要研究终点为治疗失败的时间。
结果表明,阿达木单抗对JIA相关性葡萄膜炎疗效显著,较安慰剂组显著推迟了治疗失败时间。阿达木单抗+甲氨蝶呤治疗组失败率为27%,安慰剂+甲氨蝶呤治疗组失败率为60%(HR=0.25,95%CI:0.12-0.49,P[10]。

图3 在治疗18个月期间,阿达木单抗治疗组患儿未达到治疗失败的中位治疗时间,而安慰剂组的中位治疗失败时间为24.1周
SYCAMORE研究结果还表明,阿达木单抗可帮助JIA相关性葡萄膜炎患儿实现激素减停,阿达木单抗治疗组激素成功减量及成功停药的患儿比例均显著更高(图4)[10,11]。
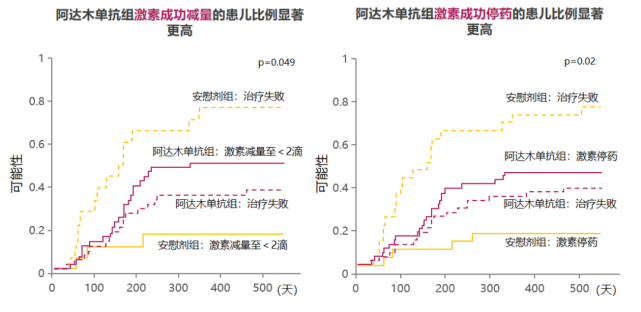
图4 阿达木单抗帮助患儿激素减停
一项回顾性研究分析了SYCAMORE研究中修美乐治疗JIA相关性葡萄膜炎的长期结局。对SYCAMORE研究中的28例患者进行复查,结果显示,在治疗1-2年停用阿达木单抗后,患者葡萄膜炎复发。该结果提示,阿达木单抗的长期持续治疗对JIA相关性葡萄膜炎患儿尤为重要[12]。
真实世界数据也表明,阿达木单抗可有效改善JIA相关性葡萄膜炎症状。来源于德国BIKER登记数据库的数据显示,自2008年阿达木单抗治疗pJIA适应症获批后使用阿达木单抗治疗的289例患儿中,仅有3.8%发生葡萄膜炎,随访期间葡萄膜炎的发生率为3.7/100患者年(py)[13]。
相对的,一项问卷调查随访纳入了德国310例应用依那西普治疗的JIA患者,收集患者应用依那西普治疗前的葡萄膜炎发生病史以及治疗后1年甚至更久的时间内葡萄膜炎发生的情况,结果显示,随访期间患儿葡萄膜炎的发生率为57/100py[14]。应用阿达木单抗后患者出现葡萄膜炎的比例相较于既往同一团队发表的应用依那西普治疗葡萄膜炎的发生比例明显更低。
结语
2019最新ACR指南指出,中/高疾病活动度或伴风险因素的多关节型幼年特发性关节炎(pJIA)患儿应及时启用生物制剂,伴高危因素的患儿可以接受生物制剂作为初始治疗[15]。

修美乐(原研阿达木单抗)为目前国内唯一获批pJIA的生物制剂,丰富了患儿的治疗选择。研究证实,长期持续的阿达木单抗治疗不仅可快速持续缓解pJIA患儿关节炎症状与体征[16-18],还可改善JIA相关葡萄膜炎等并发症,减少激素用量,维持患儿正常生长,带来更加全面的获益。
参考文献:
[1]French AR,et al.Arthritis Rheum.2001;44:523-527.
[2]Oen K, et al.J Rheumatol,2002;29:1989-1999.
[3]UmławskaW,et al.Arch Med Sci.2010;6(1):19-23.
[4]李亚琴,等.中国当代儿科杂志.2009;11(3):240-242.
[5]Wilkinson N, et al. Archives of Disease in Childhood 2003;88:186-191.
[6]Kingsbury et al. Clin Rheumatol (2014) 33:1433–1441.
[7] D. J. Lovell, et al. 2012 ACR Abstract [764]
[8]2019 American College of Rheumatology/Arthritis Foundation Guideline for the Screening, Monitoring, and Treatment of Juvenile Idiopathic Arthritis-Associated Uveitis.[J]. Arthritis Care & Research, 2019.
[9]孙利.中华实用儿科临床杂志.2018;33(9): 641-646.
[10]Ramanan AV , et al. N Engl J Med. 2017 Apr 27;376(17):1637-1646.
[11]Ramanan AV , et al. N Engl J Med. 2017 Apr 27;376(17):1637-1646. Supplementary Appendix
[12]Horton S, et al. Am J Ophthalmol. 2019. pii: S0002-9394(19)30274-0.
[13]Schmeling H, et al. Arthritis Rheum 2014; 66(9):2580-9.
[14]Schmeling H & Horneff G. Rheumatology (Oxford) 2005;44:1008–1011.
[15]Ringold S, et al. Arthritis Care Res 2019;71:717-34.
[16]Imagawa T et al. Clin Rheumatol (2012) 31:1713–1721.
[17]Lovell DJ, et al. N Engl J Med 2008;359:810–820.
[18]Lovell DJ, et al. P265. ACR 2011
专家简介

唐雪梅教授
主任医师,教授,博士,硕士生导师,重庆医科大学附属儿童医院风湿免疫科主任。
中华医学会儿科学分会免疫学组副组长中国医师协会儿科分会风湿免疫学组副组长,重庆市医学会风湿病专委会副主任委员,美国辛辛那提儿童医学中心访问学者,《中华儿科杂志》十五届通讯编委、《中华实用儿科临床杂志》编委、《儿科药学杂志》常务编委。
本材料仅供中国大陆境内的医疗卫生专业人员作为学术参考,而非针对一般公众,亦非广告用途。医疗卫生专业人员在做出任何与治疗有关的决定时,应根据患者的具体情况,参照药监局核准的药品说明书。如果您不是卫生医疗专业人士,请勿阅读和/或传播本材料。
